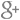 |
| ▲28일 오전 청주시 흥덕구 오송읍 식품의약품안전처에서 강석연 바이오생약국장이 의약품 성분이 뒤바뀐 골관절염 유전자치료제 '인보사케이주'(인보사)에 대한 조사 결과를 발표하고 있다. [출처=연합뉴스] |
의약품 성분이 뒤바뀐 코오롱생명과학의 골관절염 유전자치료제 '인보사케이주'(이하 인보사)의 품목허가가 취소됐다. 또 코오롱생명과학에 대해 형사고발 조치가 취해진다.
식품의약품안전처는 28일 코오롱생명과학의 골관절염 유전자 치료제 '인보사'의 주성분 중 하나가 허가 당시 제출한 자료에 기재된 연골세포가 아닌 신장세포(293유래세포)로 확인돼 품목허가를 취소한다고 밝혔다.
이에 따라 인보사는 국내 시장에서 퇴출 수순을 밟게 됐고, 코오롱생명과학은 형사고발 조치됐다.
식약처는 28일 충북 오송 식약처 브리핑실에서 '코오롱생명과학 인보사 조사 결과' 브리핑을 열고 "인보사 2액이 허가 신청 당시 제출한 자료에 기재된 연골세포가 아닌 신장세포로 확인됐고, 코오롱생명과학이 제출했던 자료가 허위로 밝혀졌다"며 이같이 말했다.
그동안 식약처는 코오롱생명과학으로부터 인보사의 성분이 뒤바뀐 경위와 이유를 증명할 수 있는 일체의 자료를 넘겨받아 조사를 펼쳤다. 인보사에 대한 자체 시험검사, 코오롱생명과학 현장조사, 미국 현지 실사 등 추가 검증도 이뤄졌다.
 |
| ▲인보사 케이주. [제공=코오롱생명과학] |
조사 결과 코오롱생명과학은 허가 당시 허위자료를 제출했고, 허가 전에 추가로 확인된 주요 사실을 숨기고 제출하지 않은 것으로 확인됐다.
인보사는 사람 연골에서 추출한 연골세포(HC)가 담긴 1액과 연골세포 성장인자(TGF-β1)를 도입한 형질전환세포(TC)가 담긴 2액을 3대1 비율로 섞어 관절강 내에 주사하는 세포 유전자 치료제다.
하지만 최근 2액 세포가 애초 식약처 허가를 받기 위해 코오롱생명과학이 제출한 자료에 기재된 '연골세포'가 아닌 '신장세포'(GP2-293세포)라는 것이 15년 만에 밝혀졌다.
식약처는 "조사 결과를 종합해 볼 때 코오롱생명과학이 인보사 허가를 위해 제출한 서류에 중대한 하자가 있는 것으로 확인됐다"며 "인보사에 대한 품목허가를 취소하고 코오롱생명과학을 형사고발하기로 했다"고 말했다.
[ⓒ 케이아이이뉴스-(구)에너지단열경제. 무단전재-재배포 금지]